
Bienvenue au Laboratoire de Chronobiologie Moléculaire! Nous étudions les bases moléculaires des rythmes circadiens, leurs liens avec la physiologie, incluant la réponse immunitaire, et leurs implications dans diverses troubles de santé, notamment la schizophrénie et les maladies infectieuses.

De nombreux processus physiologiques présentent des oscillations d’environ 24h, même en conditions constantes (1). Par exemple, les niveaux de l’hormone cortisol dans le sang sont élevés le matin, et bas le soir; un autre rythme bien caractérisé est celui de la température corporelle, élevée le jour et basse en fin de nuit chez l’humain. Ces rythmes sont appelés rythmes circadiens, et ils sont générés par des horloges circadiennes. La recherche au Laboratoire de chronobiologie moléculaire vise à étudier le fonctionnement de ces horloges, en particulier en répondant aux questions suivantes: Quels sont les mécanismes ou rouages de ces horloges? Comment ces horloges contrôlent-elles la physiologie? Comment sont-elles contrôlées par l’environnement? Qu’arrive-t-il quand les horloges se dérèglent?
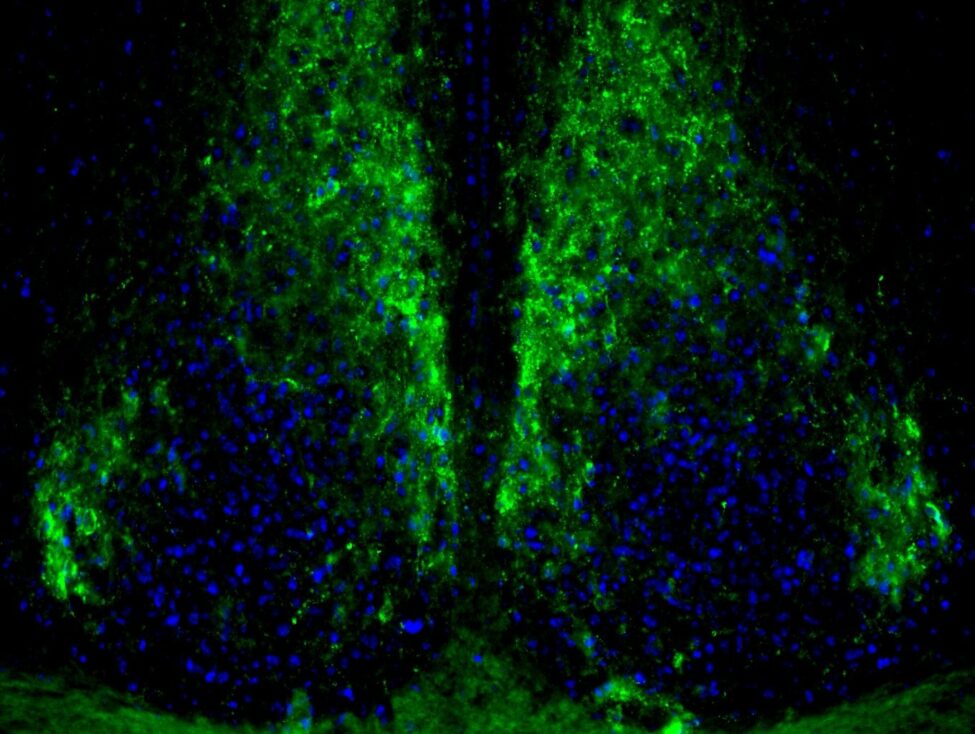
L’horloge principale chez les mammifères tels que l’humain ou la souris est située dans une région du cerveau appelée le noyau suprachiasmatique (figure). Cependant, la recherche récente a démontré que des horloges sont aussi présentes dans d’autres régions du cerveau et dans la plupart des organes périphériques. Au cours de l’évolution, les horloges ont donné un avantage aux organismes vivants, en leur permettant d’adapter leur physiologie à leur environnement aux changements cycliques (ex. cycles jour/nuit, chaud/froid), et en organisant dans le temps des processus survenant dans différents tissus. Ainsi, il n’est pas surprenant que des dérèglements des rythmes circadiens soient associés à diverses maladies, dont le cancer, les troubles métaboliques et les troubles de l’humeur.
1. Identification et étude des composantes de l’horloge
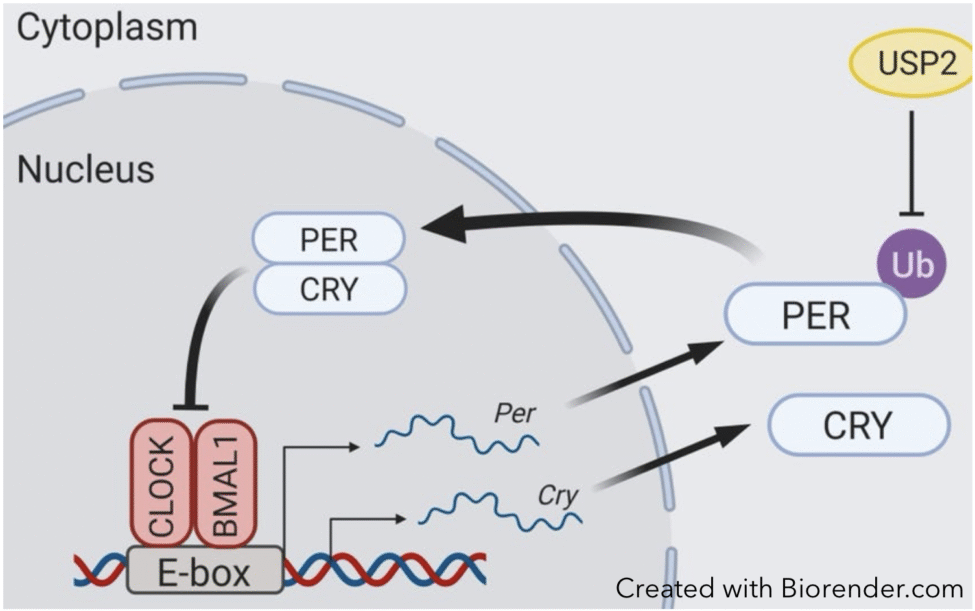
Les horloges circadiennes sont composées de gènes de l’horloge (1), et des animaux ou sujets humains avec des gènes de l’horloge mutés présentent des rythmes anormaux, ou même une arythmie dans certains cas. Au cours des années, les travaux de notre laboratoire a permis de découvrir de nouveaux gènes de l’horloge. Un exemple est la découverte que les facteurs de type REV-ERB et ROR peuvent agir comme composantes de l’horloge (2, 3). Plus récemment, nous avons étudié le rôle dans l’horloge de USP2, une protéine connue pour enlever des marques ubiquitines de protéines. En effet, l’ubiquitination de protéines de l’horloge, et leur dégradation subséquente, sont essentielles au fonctionnement de l’horloge (4). Nous avons trouvé que la réaction inverse (enlèvement de l’ubiquitine) est elle aussi importante pour l’horloge: USP2 se lie à la protéine de l’horloge PER1 et la déubiquitine, et des souris sans USP2 présentent des rythmes anormaux (figure) (5). USP2 est également impliquée dans la réponse de l’horloge à la lumière (6).
2. Le contrôle circadien de la réponse immunitaire et des maladies infectieuses
Les horloges circadiennes sont retrouvées partout dans l’organisme, incluant dans les cellules du système immunitaire (7). Est-ce que ceci veut dire que l’immunité est plus ou moins efficace selon l’heure du jour? En collaboration avec Dr. Nathalie Labrecque (IRCM, Université de Montréal), nous avons découvert que c’est le cas: la réponse à la vaccination varie selon l’heure du jour. Lorsque des souris reçoivent le traitement en milieu de jour, leur lymphocytes T répondent plus fortement à la présentation de l’antigène qu’à toutes autres heures du jour et de la nuit (8, 9). Des souris qui n’ont pas d’horloge circadienne des lymphocytes T ne présentent pas ce rythme circadien. Notre analyse des rythmes moléculaires dans les lymphocytes T nous a ensuite permis de conclure que ces cellules sont réglées (par une horloge qui leur est propre) pour être prêtes à répondre efficacement le jour, et pour être plus résistantes à la vaccination la nuit (9, 10).
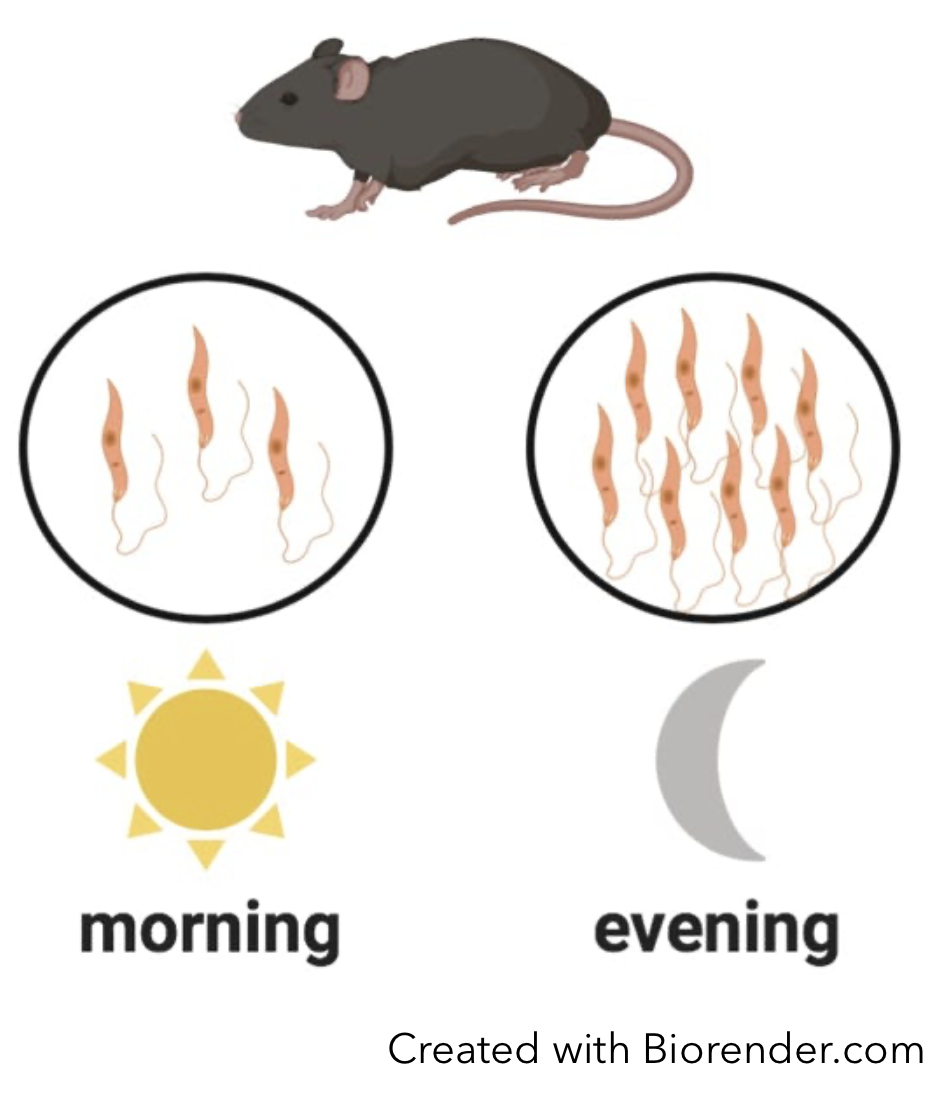
Quel est l’impact des rythmes du système immunitaire pour la lutte contre les maladies infectieuses? En collaboration avec Dr. Martin Olivier (IR-CUSM, Université McGill), nous tentons de répondre à cette question dans le cadre d’infections parasitaires (11, 12). Le parasite Leishmania cause la leishmaniose, une maladie grave très courante en particulier dans les régions tropicales. Nous avons découvert que la réponse immunitaire varie selon l’heure du jour à laquelle le parasite est inoculé à des souris (figure): une infection en soirée mène à une mobilisation plus forte de cellules du système immunitaire, et comme le parasite a besoin de ces cellules pour se reproduire, une infection en soirée est bénéfique pour le parasite, qui se divise alors plus fortement (13). Nous avons aussi démontré un rythme circadien de l’infection par Plasmodium, le parasite donnant le paludisme (14, 15). Pour les deux parasites, les horloges des cellules immunitaires, en particulier des macrophages, est importante pour le contrôle circadien (10, 15, 16).
3. Dérèglements circadiens et schizophrénie
Environ 80% des patients souffrant de schizophrénie présentent des troubles du sommeil et des rythmes circadiens (17, 18). En collaboration avec Dr. Lalit Srivastava (Centre de recherche Douglas, Université McGill), nous nous posons deux questions. Premièrement, quelle est la cause de ces troubles des rythmes circadiens? Deuxièmement, est-ce que des dérèglements des rythmes pourraient aggraver les symptômes de la schizophrénie, ou agir comme un facteur de risque pour développer la maladie, ainsi que d’autres qui sont aussi causées par un dévelopment anormal du cerveau (17, 18)? Pour répondre à ces questions, nous utilisons des modèles animaux. Par exemple, nous avons démontré que des souris avec une mutation du gène de la Dysbindine-1 (qui est associé à la schizophrénie) présentent des rythmes circadiens anormaux (19). De plus, des conditions de lumière qui dérèglent les rythmes des souris intensifient des comportements similaires à la schizophrénie chez ces souris mutantes (19, 20). Nous avons également étudié un modèle de souris d’infection prénatale, qui est un facteur de risque bien connu de troubles du développement du cerveau: ici aussi, nous avons observé des rythmes altérés, et des dérèglements circadiens sont associés avec des caractéristiques des maladies (21, 22). Ces travaux pourraient permettre de développer de nouvelles stratégies prenant en compte les rythmes circadiens, pour améliorer la cognition des patients avec schizophrénie et autres troubles psychiatriques. D’ailleurs, nous utilisons maintenant les données collectées chez les souris pour étudier le risque de troubles psychiatriques dans les populations humaines (avec Dr. Patricia Silveira, Douglas, McGill).

4. La régulation des horloges circadiennes humaines: implications pour le travail de nuit
Afin d’étudier la régulation des horloges circadiennes chez l’humain, nous nous sommes associés avec Dr. Diane Boivin (Centre de recherche Douglas, Université McGill). Par des études de simulation de travail de nuit en laboratoire, et des études de terrain avec des travailleurs de nuit, nous avons démontré que tout comme l’horloge centrale, les horloges périphériques humaines ne s’adaptent pas bien à un horaire de nuit (23, 24). La conséquence de cela est un manque de synchronisation des rythmes moléculaires (23-25), immunitaire (26) et métaboliques (27, 28). Nous avons aussi fait la toute première démonstration d’un ajustement pharmacologique des horloges périphériques chez l’humain (29). Enfin, nous nous sommes aussi intéressés à l’expression des gènes de l’horloge dans le tissu cérébral post-mortem, et nous avons trouvé que les rythmes d’expression des gènes de l’horloge étaient différents chez les patients de la maladie Alzheimer par rapport à des sujets contrôles, ce qui pourrait être à l’origine des problèmes de sommeil et de rythmes circadiens chez ces patients (30).
1. Duguay, D. & Cermakian, N. (2009) Chronobiol Int 26, 1479-513. 2. Guillaumond, F., Dardente, H., Giguère, V. & Cermakian, N. (2005) J Biol Rhythms 20, 391-403. 3. Mongrain, V., Ruan, X., Dardente, H., Fortier, E. E. & Cermakian, N. (2008) Genes Cells 13, 1197-210. 4. Stojkovic, K., Wing, S.S., Cermakian, N. (2014) Front Mol Neurosci, 7:69. 5. Yang, Y. et al. (2012) Biol Open, 1:789-801. 6. Srikanta, S.B., (…) Cermakian, N. (2025) J Neurochem, 169:e70018. 7. Nobis, C.C., Labrecque, N., Cermakian, N. (2018) Curr Opin Physiol, 5:90-98. 8. Fortier, E.E. et al. (2011) J Immunol 187:6291-300. 9. Nobis, C.C., (…) Cermakian, N. (2019) Proc Natl Acad Sci USA, 1;116(40):20077-20086. 10. Cermakian, N., Labrecque, N. (2023) J Immunol, 210:12–18. 11. Carvalho Cabral, P., Olivier, M., Cermakian, N. (2019) The Complex Interplay of Parasites, their Hosts and Circadian Clocks. Front Cell Infect Microbiol, 9:425. 12. Carvalho Cabral, P., Tekade, K., Stegeman, S.K., Olivier, M., Cermakian, N. (2022) Par Immunol, 44:e12903. 13. Kiessling, S., Dubeau-Laramée, G., Ohm, H., Labrecque, N., Olivier, M., Cermakian, N. (2017) Sci Rep, 7:10892. 14. Carvalho Cabral, P., Weinerman, J., Olivier, M., Cermakian, N. (2024) iScience, 27:109684. 15. Carvalho Cabral, P., Richard, V.R., Borchers, C.H., Olivier, M., Cermakian, N. (2024) ImmunoHorizons, 8(6):442–456. 16. Carvalho Cabral, P., Stegeman, S.K., Olivier, M., Cermakian, N. (2024) Par Immunol, 46:e13053. 17. Delorme, T.C., Srivastava, L.K., Cermakian, N. (2020) Journal of Biological Rhythms, 35(4):325-339. 18. Bouteldja, A.A., Penichet, D., Srivastava, L.K., Cermakian, N. (2024) European Journal of Neuroscience, 60:3858–3890. 19. Bhardwaj, S.K., Stojkovic, K., Kiessling, S., Srivastava, L.K., Cermakian, N. (2015) Behav Brain Res, 284:58-68. 20. Cloutier, M.E., Srivastava, L.K., Cermakian, N. (2022) J Biol Rhythms, 37(6):655-672. 21. Delorme, T.C., Srivastava, L.K., Cermakian, N. (2021) Brain Behav Immun, 93:119-131. 22. Delorme, T., (…) Cermakian, N. (2025) Brain Behav Immun, 127:409-422. 23. Cuesta, M., Boudreau, P., Cermakian, N., Boivin, D.B. (2017) Sci Rep, 7:16310. 24. Koshy, A., Cuesta, M., Boudreau, P., Cermakian, N., Boivin, D.B. (2019) FASEB Journal, 33(6):6789-6800. 25. Kervezee, L., Cuesta, M., Cermakian, N., Boivin, D.B. (2018) Proc Natl Acad Sci USA, 115(21):5540-5545. 26. Cuesta, M., Boudreau, P., Dubeau-Laramée, G., Cermakian, N., Boivin, D.B. (2016) J Immunol, 196(6):2466-75. 27. Kervezee, L., Cermakian, N., Boivin, D.B. (2019) PLOS Biol, 18;17(6):e3000303. 28. Kervezee, L., Koshy, A., Cermakian, N., Boivin, D.B. (2023) J Biol Rhythms, 38:64-76. 29. Cuesta, M., Cermakian, N., Boivin, D.B. (2015) FASEB J, 29(4):1360-70. 30. Cermakian, N., Waddington Lamont, E., Boudreau, P. & Boivin, D.B. (2011) J Biol Rhythms 26, 160-170.
Ce contenu a été mis à jour le 3 février 2026 à 15h35.